Daptar Eusi Pikeun Artikel ieu:
1. Kamekaran Asam Amino
2. Sipat struktural
3. Komposisi kimiawi
4. Klasifikasi
5. Sintésis
6. Sipat fisikokimia
7. Karacunan
8. aktivitas antimikrobial
9. Sipat réologis
10. Aplikasi dina industri kosmetik
11. Aplikasi dina kosmétik sapopoé
Surfaktan Asam Amino (AAS)nyaéta kelas surfaktan nu dibentuk ku ngagabungkeun gugus hidrofobik jeung hiji atawa leuwih Asam Amino.Dina hal ieu, Asam Amino tiasa sintétik atanapi diturunkeun tina hidrolisat protéin atanapi sumber anu tiasa diperbaharui.Tulisan ieu nyertakeun detil seueur rute sintétik anu sayogi pikeun AAS sareng pangaruh rute anu béda dina sipat fisikokimia produk ahir, kalebet kalarutan, stabilitas dispersi, karacunan sareng biodegradabilitas.Salaku kelas surfactants dina ngaronjatkeun paménta, versatility of AAS alatan struktur variabel maranéhna nawarkeun angka nu gede ngarupakeun kasempetan komérsial.
Kusabab surfaktan loba dipaké dina detergents, émulsifiers, sambetan korosi, recovery minyak tersiér jeung farmasi, peneliti geus pernah ceased nengetan surfactants.
Surfactants mangrupikeun produk kimia anu paling representatif anu dikonsumsi dina jumlah anu ageung unggal dinten di sakumna dunya sareng ngagaduhan dampak negatif kana lingkungan akuatik.Studi geus ditémbongkeun yén pamakéan nyebar surfaktan tradisional bisa boga dampak negatif kana lingkungan.
Kiwari, non-toksik, biodegradabilitas sareng biokompatibilitas ampir sami pentingna pikeun konsumén salaku utilitas sareng kinerja surfaktan.
Biosurfaktan nyaéta surfaktan sustainable anu ramah lingkungan anu disintésis sacara alami ku mikroorganisme sapertos baktéri, fungi, sareng ragi, atanapi disékrésikeun sacara ékstrasélular.Ku alatan éta, biosurfaktan ogé bisa disiapkeun ku desain molekul pikeun meniru struktur amphiphilic alam, kayaning fosfolipid, alkil glikosida jeung asil Asam Amino.
Surfaktan Asam Amino (AAS)mangrupa salah sahiji surfaktan has, biasana dihasilkeun tina sato atawa bahan baku agriculturally diturunkeun.Sapanjang dua dasawarsa katukang, AAS parantos narik minat para ilmuwan salaku surfaktan novél, sanés ngan kusabab aranjeunna tiasa disintésis tina sumber daya anu tiasa dianyari, tapi ogé kusabab AAS gampang terurai sareng gaduh produk sampingan anu teu bahaya, ngajantenkeun aranjeunna langkung aman pikeun lingkungan.
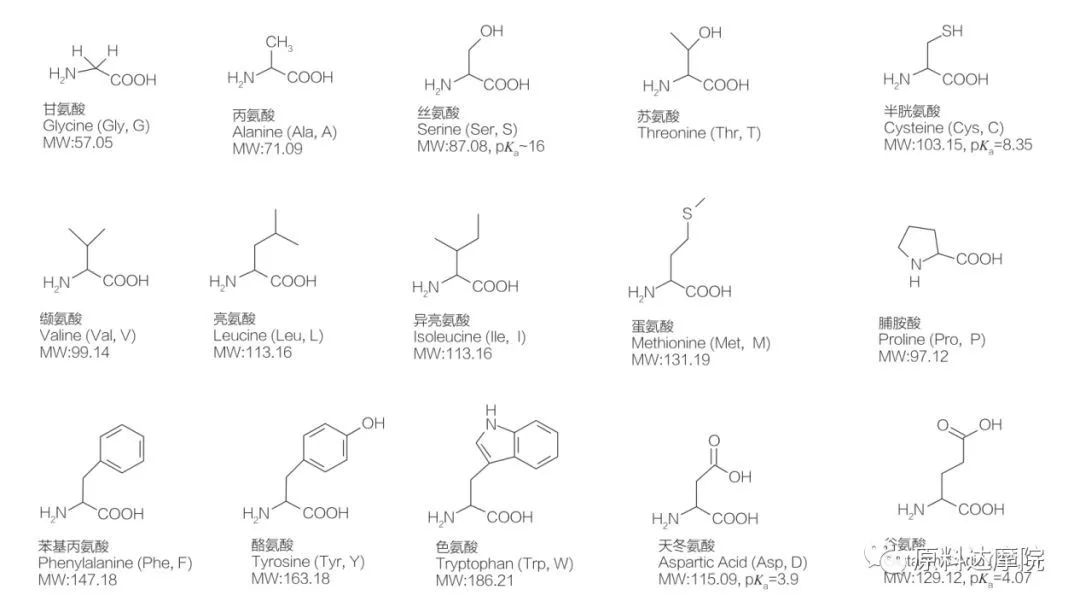
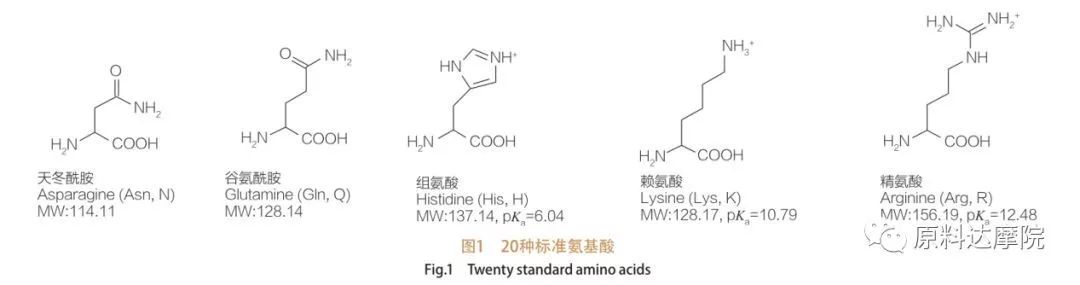
AAS bisa dihartikeun minangka kelas surfaktan nu diwangun ku Asam Amino nu ngandung gugus Asam Amino (HO 2 C-CHR-NH 2) atawa résidu Asam Amino (HO 2 C-CHR-NH-).2 wewengkon fungsional Asam Amino ngamungkinkeun pikeun turunan rupa-rupa surfaktan.Jumlahna aya 20 Asam Amino Protéinogenik standar anu dipikanyaho aya di alam sareng tanggung jawab kana sadaya réaksi fisiologis dina kagiatan pertumbuhan sareng kahirupan.Maranéhanana béda ti silih ngan nurutkeun résidu R (Gambar 1, pk a logaritma négatip tina konstanta disosiasi asam leyuran).Aya anu non-polar sareng hidrofobik, aya anu polar sareng hidrofilik, aya anu basa sareng aya anu asam.
Kusabab Asam Amino mangrupikeun sanyawa anu tiasa dianyari, surfaktan anu disintésis tina Asam Amino ogé ngagaduhan poténsi anu luhur pikeun janten sustainable sareng ramah lingkungan.Struktur basajan tur alam, karacunan low sarta biodegradability gancang mindeng ngajadikeun eta leuwih unggul ti surfactants konvensional.Ngagunakeun bahan baku renewable (misalna Asam Amino jeung minyak nabati), AAS bisa dihasilkeun ku rute biotéhnologis béda jeung jalur kimiawi.
Dina awal abad ka-20, Asam Amino munggaran kapanggih pikeun dipaké salaku substrat pikeun sintésis surfaktan.AAS utamana dipaké salaku pengawet dina formulasi farmasi sarta kosmetik.Salaku tambahan, AAS kapanggih sacara biologis aktip ngalawan rupa-rupa baktéri, tumor, sareng virus anu nyababkeun panyakit.Dina 1988, kasadiaan AAS béaya rendah ngahasilkeun minat panalungtikan dina kagiatan permukaan.Kiwari, ku ngembangkeun biotéhnologi, sababaraha Asam Amino ogé tiasa disintésis sacara komersil dina skala ageung ku ragi, anu sacara henteu langsung ngabuktikeun yén produksi AAS langkung ramah lingkungan.
01 Pangwangunan Asam Amino
Awal abad ka-19, nalika Asam Amino alami munggaran kapanggih, strukturna diprediksi pisan berharga - tiasa dianggo salaku bahan baku pikeun persiapan amphiphiles.Ulikan munggaran ngeunaan sintésis AAS dilaporkeun ku Bondi taun 1909.
Dina ulikan éta, N-asilglisin jeung N-asilalanine diwanohkeun minangka gugus hidrofilik pikeun surfaktan.Karya saterasna ngalibatkeun sintésis asam lipoAmino (AAS) nganggo glisin sareng alanin, sareng Hentrich dkk.diterbitkeun runtuyan papanggihan,kaasup aplikasi patén munggaran, dina pamakéan acyl sarcosinate na acyl aspartate uyah salaku surfaktan dina produk beberesih rumah tangga (misalna shampoos, detergents jeung odol).Satuluyna, loba peneliti nalungtik sintésis jeung sipat fisikokimia asam amino asil.Nepi ka ayeuna, sajumlah ageung literatur parantos diterbitkeun ngeunaan sintésis, sipat, aplikasi industri sareng biodegradabilitas AAS.
02 Sipat Struktural
Ranté asam lemak hidrofobik non-polar AAS tiasa béda-béda dina struktur, panjang ranté sareng jumlah.Keragaman struktural sareng aktivitas permukaan luhur AAS ngajelaskeun karagaman komposisi anu lega sareng sipat fisikokimia sareng biologis.Gugus kapala AAS diwangun ku Asam Amino atawa péptida.Bedana dina grup sirah nangtukeun adsorption, aggregation jeung aktivitas biologis surfactants ieu.Gugus fungsi dina gugus sirah lajeng nangtukeun jenis AAS, kaasup kationik, anionik, nonionic, jeung amphoteric.Kombinasi Asam Amino hidrofilik sareng bagian ranté panjang hidrofobik ngabentuk struktur amphiphilic anu ngajantenkeun molekul éta aktip pisan di permukaan.Sajaba ti éta, ayana atom karbon asimétri dina molekul mantuan pikeun ngabentuk molekul kiral.
03 Komposisi Kimia
Sadaya Péptida sareng Polipéptida mangrupikeun produk Polimérisasi tina ampir 20 Asam α-Protéinogenik α-Amino ieu.Sakabéh 20 Asam α-Amino ngandung gugus fungsi asam karboksilat (-COOH) jeung gugus fungsi amino (-NH 2), duanana napel kana atom α-karbon tétrahedral nu sarua.Asam Amino béda-béda ku gugus-gugus R anu béda-béda napel kana α-karbon (iwal lisin, dimana gugus R nyaéta hidrogén.) Gugus R bisa béda dina struktur, ukuran jeung muatan (kaasaman, alkalinitas).Bédana ieu ogé nangtukeun kaleyuran Asam Amino dina cai.
Asam Amino mangrupakeun kiral (iwal glisin) jeung sacara optik aktip ku alam sabab mibanda opat substituén béda numbu ka karbon alfa.Asam Amino gaduh dua konformasi anu mungkin;aranjeunna gambar eunteung non-tumpang tindih saling, sanajan kanyataan yén jumlah L-stereoisomer nyata leuwih luhur.Gugus-R anu aya dina sababaraha Asam Amino (Phenylalanine, Tyrosine and Tryptophan) nyaéta aril, ngarah nyerep UV maksimum dina 280 nm.Asam α-COOH jeung α-NH 2 dasar dina Asam Amino sanggup ionisasi, sarta duanana stereoisomer, nu mana wae aranjeunna, ngawangun kasatimbangan ionisasi ditémbongkeun di handap.
R-COOH ↔R-COO-+H+
R-NH3+↔R-NH2+H+
Saperti ditémbongkeun dina kasatimbangan ionisasi di luhur, asam amino ngandung sahenteuna dua gugus asam lemah;kumaha oge, gugus karboksil leuwih asam dibandingkeun jeung gugus amino nu diprotonasi.pH 7,4, gugus karboksil deprotonasi sedengkeun gugus amino diprotonasi.Asam amino jeung gugus R non-ionizable sacara listrik nétral dina pH ieu sarta ngabentuk zwitterion.
04 Klasifikasi
AAS tiasa digolongkeun dumasar kana opat kritéria, anu dijelaskeun di handap.
4.1 Numutkeun asal
| Nurutkeun asal-usulna, AAS bisa dibagi jadi 2 kategori saperti ieu di handap. ① Kategori Alam Sababaraha sanyawa alami anu ngandung asam amino ogé gaduh kamampuan pikeun ngirangan tegangan permukaan / antarmuka, sareng sababaraha malah ngaleuwihan khasiat glikolipid.AAS ieu ogé katelah lipopéptida.Lipopéptida nyaéta sanyawa beurat molekul rendah, biasana dihasilkeun ku spésiés Bacillus.
AAS sapertos kitu dibagi deui kana 3 subclass:surfactin, iturin sareng fengycin.
|
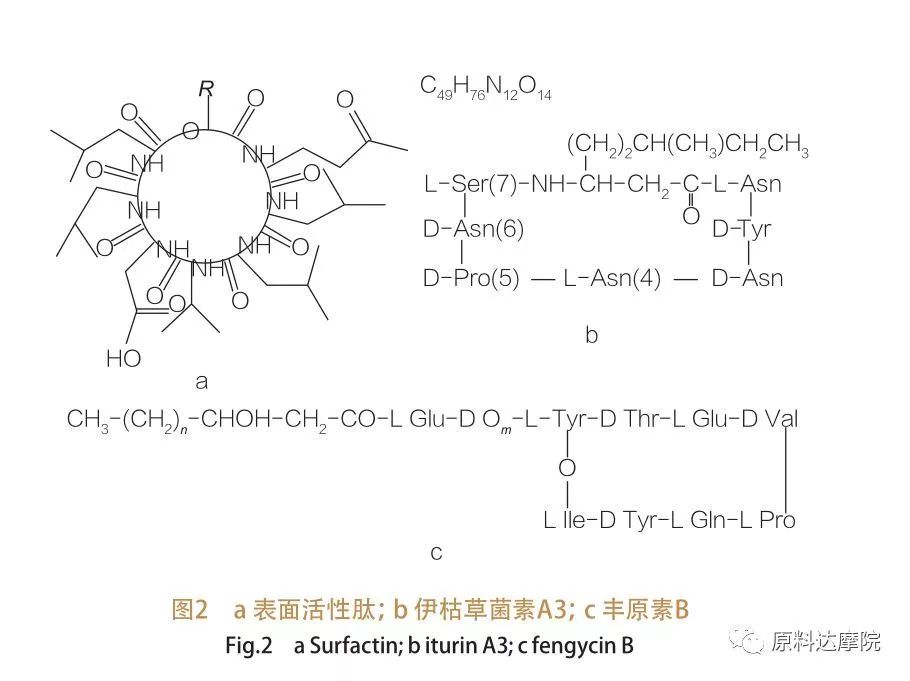
| Kulawarga péptida aktif permukaan ngawengku varian héptapéptida tina rupa-rupa zat,ditémbongkeun saperti dina Gambar 2a, dimana ranté asam lemak β-hidroksi C12-C16 teu jenuh numbu ka péptida.Péptida aktip-permukaan nyaéta lakton makrosiklik dimana cincinna ditutup ku katalisis antara terminal C asam lemak β-hidroksi sareng péptida. Dina subkelas iturin, aya genep varian utama, nyaéta iturin A jeung C, mycosubtilin jeung bacillomycin D, F jeung L.Dina sagala hal, héptapéptida numbu ka ranté C14-C17 asam lemak β-amino (ranténa bisa rupa-rupa).Dina kasus ékurimisin, gugus amino dina posisi β tiasa ngabentuk beungkeut amida sareng terminal C sahingga ngabentuk struktur laktam makrosiklik.
Subkelas fengycin ngandung fengycin A jeung B, nu disebut oge plistatin nalika Tyr9 D-konpigurasi.Dékapéptida dikaitkeun kana ranté asam lemak β-hidroksi C14-C18 jenuh atawa teu jenuh.Sacara stuktur, plipastatin ogé mangrupa lakton makrosiklik, ngandung ranté samping Tyr dina posisi 3 tina runtuyan péptida sarta ngabentuk beungkeut éster jeung résidu C-terminal, sahingga ngabentuk struktur cingcin internal (sakumaha dina kasus loba Pseudomonas lipopeptides).
② Kategori sintétik AAS ogé bisa disintésis ku ngagunakeun salah sahiji asam amino asam, basa jeung nétral.Asam amino anu umum dianggo pikeun sintésis AAS nyaéta asam glutamat, serin, prolin, asam aspartat, glisin, arginin, alanin, leusin, sareng hidrolisat protéin.Subkelas surfaktan ieu tiasa disiapkeun ku cara kimia, énzimatik, sareng kémoénzimatik;kumaha oge, pikeun produksi AAS, sintésis kimiawi leuwih ekonomis meujeuhna.Conto umum nyaéta asam N-lauroyl-L-glutamat sareng asam N-palmitoyl-L-glutamat.
|
4.2 Dumasar substituén ranté alifatik
Dumasar substituén ranté alifatik, surfaktan dumasar-asam amino bisa dibagi jadi 2 jenis.
Nurutkeun posisi substituent
| ①N-diganti AAS Dina sanyawa anu disubstitusi N, gugus amino diganti ku gugus lipofilik atawa gugus karboksil, ngabalukarkeun leungitna basa.conto pangbasajanna N-substituted AAS nyaéta asam amino N-asil, nu dasarna surfaktan anionik.N-substituted AAS boga beungkeut amida napel antara porsi hidrofobik jeung hidrofilik.Beungkeut amida mibanda kamampuhan pikeun ngabentuk beungkeut hidrogén, nu ngagampangkeun degradasi surfaktan ieu dina lingkungan asam, sahingga ngajadikeun biodegradable.
②C-diganti AAS Dina sanyawa anu disubstitusi C, substitusi lumangsung dina gugus karboksil (ngaliwatan beungkeut amida atawa éster).Sanyawa anu disubstitusi-C (contona éster atanapi amida) dasarna mangrupikeun surfaktan kationik.
③N- jeung C-diganti AAS Dina jenis surfaktan ieu, gugus amino sareng karboksil mangrupikeun bagian hidrofilik.Jenis ieu dasarna mangrupa surfaktan amphoteric. |
4.3 Nurutkeun jumlah buntut hidrofobik
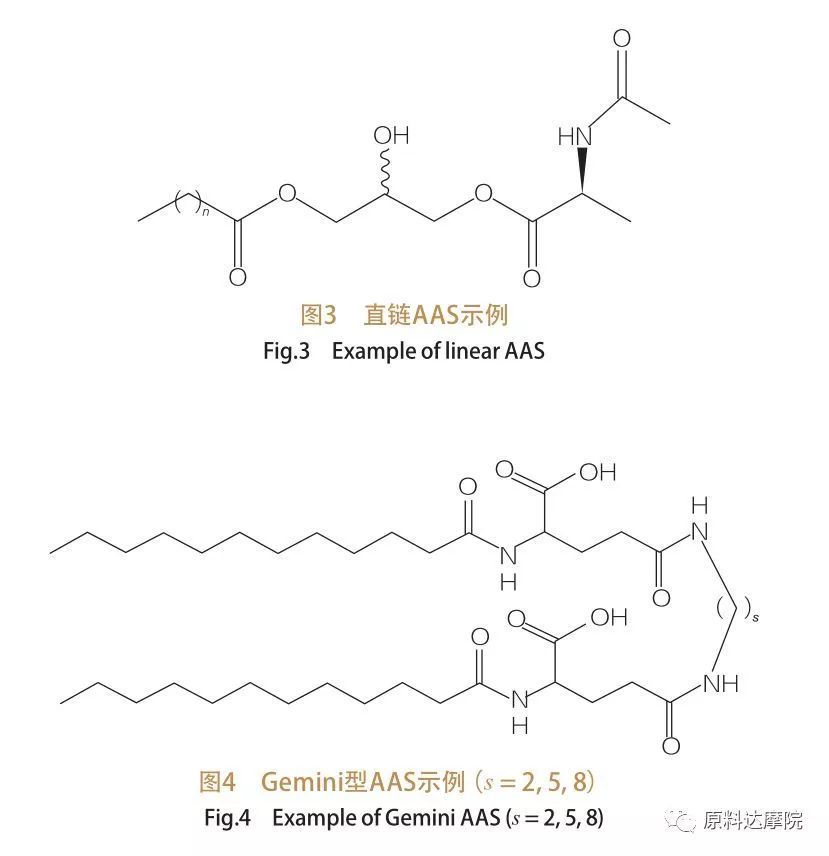
Dumasar jumlah gugus hulu jeung buntut hidrofobik, AAS bisa dibagi jadi opat golongan.Straight-chain AAS, Gemini (dimer) type AAS, Glycerolipid type AAS, and bicephalic amphiphilic (Bola) type AAS.surfaktan ranté lempeng nyaéta surfaktan nu diwangun ku asam amino kalawan ngan hiji buntut hidrofobik (Gambar 3).Gemini tipe AAS boga dua asam amino gugus sirah polar jeung dua buntut hidrofobik per molekul (Gambar 4).Dina tipe ieu struktur, dua ranté lempeng AAS numbu babarengan ku spacer sahingga disebut ogé dimer.Dina tipe Glycerolipid AAS, di sisi séjén, dua buntut hidrofobik napel na gugus sirah asam amino sarua.Surfaktan ieu bisa dianggap minangka analog tina monogliserida, digliserida jeung fosfolipid, sedengkeun dina AAS tipe Bola, dua gugus hulu asam amino dihijikeun ku buntut hidrofobik.
4.4 Nurutkeun jenis kelompok kapala
①Kationik AAS
Grup sirah tina tipe ieu surfactant boga muatan positif.AAS kationik pangheubeulna nyaéta étil cocoyl arginate, nyaéta pirolidon karboksilat.Sipat unik sareng rupa-rupa surfaktan ieu ngajantenkeun mangpaat dina disinféktan, agén antimikroba, agén antistatik, kondisioner rambut, ogé lemes dina panon sareng kulit sareng gampang biodegradable.Singare sareng Mhatre nyintésis AAS kationik dumasar-arginin sareng ngaevaluasi sipat fisikokimiana.Dina ulikan ieu, maranéhna ngaku ngahasilkeun tinggi tina produk diala ngagunakeun kaayaan réaksi Schotten-Baumann.Kalayan ngaronjatna panjang ranté alkil jeung hidrofobik, aktivitas permukaan surfaktan kapanggih ngaronjat sarta Konsentrasi Micelle Kritis (cmc) ngurangan.Anu sanésna nyaéta protéin asil kuarterner, anu biasa dianggo salaku kondisioner dina produk perawatan rambut.
②Aionic AAS
Dina surfaktan anionik, gugus sirah polar surfaktan boga muatan négatip.Sarcosine (CH 3 -NH-CH 2 -COOH, N-methylglycine), asam amino nu ilahar kapanggih dina landak laut jeung béntang laut, sacara kimiawi aya hubunganana jeung glisin (NH 2 -CH 2 -COOH,), asam amino dasar kapanggih. dina sél mamalia.-COOH,) sacara kimiawi aya hubunganana sareng glisin, nyaéta asam amino dasar anu aya dina sél mamalia.Asam laurat, asam tetradekanoat, asam oleat sareng halida sareng ésterna biasana dianggo pikeun nyintésis surfaktan sarkosinat.Sarcosinates sipatna hampang sahingga ilahar dipaké dina mouthwashes, shampoos, semprot busa cukur, sunscreens, cleansers kulit, sarta produk kosmetik lianna.
AAS anionik séjén anu sayogi sacara komersil kalebet Amisoft CS-22 sareng AmiliteGCK-12, anu mangrupikeun nami dagang natrium N-cocoyl-L-glutamat sareng kalium N-cocoyl glycinate, masing-masing.Amilite ilaharna dipaké salaku agén foaming, detergent, solubilizer, emulsifier na dispersant, sarta ngabogaan loba aplikasi dina kosmétik, kayaning shampoos, sabun mandi, washes awak, odol, cleansers raray, cleansing sabun, cleaners lénsa kontak jeung surfactants rumah tangga.Amisoft dipaké salaku cleanser kulit jeung bulu hampang, utamana dina cleansers raray jeung awak, block detergents sintétik, produk perawatan awak, shampoos jeung produk perawatan kulit lianna.
③zwitterionic atanapi amphoteric AAS
Surfaktan amfotérik ngandung situs asam jeung basa, sahingga bisa ngarobah muatanana ku cara ngarobah nilai pH.Dina media basa aranjeunna kalakuanana sapertos surfaktan anionik, sedengkeun dina lingkungan asam aranjeunna kalakuanana sapertos surfaktan kationik sareng dina media nétral sapertos surfaktan amfoterik.Lauryl lisin (LL) jeung alkoksi (2-hydroxypropyl) arginin nyaéta hiji-hijina surfaktan amfotérik dumasar kana asam amino.LL mangrupikeun produk kondensasi lisin sareng asam laurat.Kusabab struktur amfotérikna, LL teu leyur dina ampir kabéh jenis pangleyur, iwal ti pangleyur anu basa atawa asam pisan.Salaku bubuk organik, LL ngabogaan adhesion alus teuing pikeun surfaces hidrofilik sarta koefisien gesekan low, méré surfactant ieu kamampuhan lubricating alus teuing.LL seueur dianggo dina krim kulit sareng kondisioner rambut, sareng ogé dianggo salaku pelumas.
④AAS nonionik
Surfaktan nonionik dicirikeun ku gugus sirah polar tanpa muatan formal.dalapan surfaktan nonionik ethoxylated anyar anu disiapkeun ku Al-Sabagh et al.tina asam α-amino larut minyak.Dina prosés ieu, L-phenylalanine (LEP) jeung L-leucine munggaran diésterifikasi ku héksadékanol, dituturkeun ku amidasi jeung asam palmitat pikeun méré dua amida jeung dua éster asam α-amino.Amida sareng éster teras ngalaman réaksi kondensasi sareng étiléna oksida pikeun nyiapkeun tilu turunan fénilalanin kalayan jumlah unit polioksiétilén anu béda (40, 60 sareng 100).AAS nonionik ieu kapanggih boga detergénsi alus sarta sipat foaming.
05 Sintésis
5.1 Rute sintétik dasar
Dina AAS, gugus hidrofobik bisa napel kana amina atawa situs asam karboksilat, atawa ngaliwatan ranté samping asam amino.Dumasar ieu, aya opat rute sintétik dasar, sapertos anu dipidangkeun dina Gambar 5.
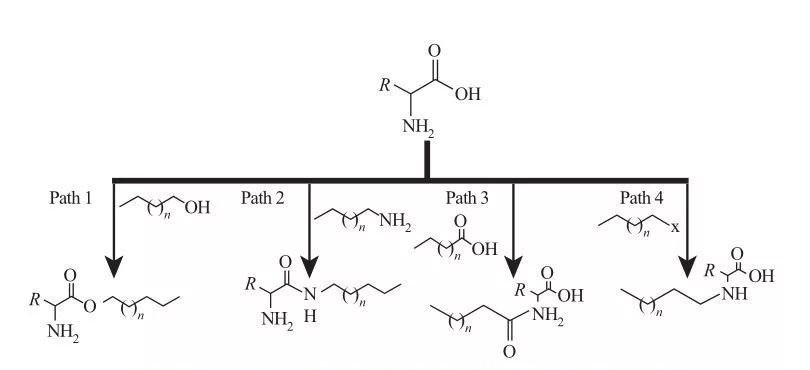
Gbr.5 Jalur sintésis dasar surfaktan dumasar-asam amino
| Jalur 1. Amina éster amphifilik dihasilkeun ku réaksi ésterifikasi, dina hal ieu sintésis surfaktan biasana kahontal ku réfluks alkohol lemak jeung asam amino ku ayana agén dehidrasi jeung katalis asam.Dina sababaraha réaksi, asam sulfat bertindak salaku katalis sareng agén dehidrasi.
Jalur 2. Asam amino anu diaktipkeun ngaréaksikeun sareng alkilamin pikeun ngabentuk beungkeut amida, nyababkeun sintésis amidoamina amfifilik.
Jalur 3. Asam Amido disintésis ku ngaréaksikeun gugus amina asam amino jeung Asam Amido.
Jalur 4. Asam amino alkil ranté panjang disintésis ku réaksi gugus amina jeung haloalkana. |
5.2 Kamajuan dina sintésis jeung produksi
5.2.1 Sintésis asam amino tunggal-ranté / surfaktan péptida
Asam amino N-asil atanapi O-asil atanapi péptida tiasa disintésis ku asilasi énzim-katalisis gugus amina atanapi hidroksil sareng asam lemak.Laporan pangheubeulna ngeunaan sintésis lipase-katalisis bébas-pangleyur tina asam amino amida atawa turunan métil éster dipaké Candida antarctica, kalawan ngahasilkeun mimitian ti 25% nepi ka 90% gumantung kana target asam amino.Métil étil keton ogé geus dipaké salaku pangleyur dina sababaraha réaksi.Vonderhagen et al.ogé ngajelaskeun réaksi N-asilasi lipase jeung protease-katalis asam amino, hidrolisat protéin jeung/atawa turunanna maké campuran cai jeung pangleyur organik (misalna dimétilformamida/cai) jeung métil butil keton.
Dina poé mimiti, masalah utama jeung sintésis énzim-katalisis AAS nya éta ngahasilkeun low.Numutkeun Valivety et al.ngahasilkeun turunan asam amino N-tetradecanoyl éta ngan 2% -10% malah sanggeus ngagunakeun lipase béda jeung incubating dina 70 ° C salila sababaraha poé.Montet et al.ogé ngalaman masalah ngeunaan kurangna ngahasilkeun asam amino dina sintésis N-asil lisin maké asam lemak jeung minyak nabati.Numutkeun aranjeunna, ngahasilkeun maksimum produk éta 19% dina kaayaan bébas pangleyur sarta ngagunakeun pangleyur organik.masalah anu sarua ieu encountered ku Valivety et al.dina sintésis N-Cbz-L-lisin atawa N-Cbz-lisin turunan métil éster.
Dina ulikan ieu, maranéhna ngaku yén ngahasilkeun 3-O-tetradecanoyl-L-serine éta 80% lamun ngagunakeun N-ditangtayungan serine salaku substrat jeung Novozyme 435 salaku katalis dina lingkungan lebur pangleyur-gratis.Nagao sareng Kito ngulik O-asilasi L-serin, L-homoserin, L-treonin sareng L-tirosin (LET) nalika nganggo lipase Hasil réaksina (lipase dicandak ku Candida cylindracea sareng Rhizopus delemar dina médium panyangga cai) sarta dilaporkeun yén ngahasilkeun acylation of L-homoserine na L-serine éta rada low, bari euweuh acylation of L-threonine na LET lumangsung.
Loba peneliti geus ngarojong pamakéan substrat murah tur gampang sadia pikeun sintésis AAS ongkos-éféktif.Soo et al.ngaku yén persiapan surfaktan basis minyak sawit jalan pangalusna kalawan lipoenzyme immobilized.Aranjeunna nyatet yén ngahasilkeun produk bakal langkung saé sanaos réaksi anu nyéépkeun waktos (6 dinten).Gerova et al.nalungtik sintésis jeung aktivitas permukaan kiral N-palmitoyl AAS dumasar kana methionine, prolin, leusin, threonine, fenilalanin jeung phenylglycine dina campuran siklik / racemic.Pang jeung Chu ngajéntrékeun sintésis monomér dumasar asam amino jeung monomér dumasar asam dikarboksilat dina leyuran Runtuyan éster poliamida basis asam amino fungsional jeung biodegradable disintésis ku réaksi ko-kondensasi dina leyuran.
Cantaeuzene sareng Guerreiro ngalaporkeun ésterifikasi gugus asam karboksilat Boc-Ala-OH sareng Boc-Asp-OH kalayan alkohol alifatik rantai panjang sareng diol, kalayan diklorometana salaku pangleyur sareng agarose 4B (Sepharose 4B) salaku katalis.Dina ulikan ieu, réaksi Boc-Ala-OH jeung alkohol lemak nepi ka 16 karbon méré hasil alus (51%), sedengkeun pikeun Boc-Asp-OH 6 jeung 12 karbon leuwih alus, kalawan ngahasilkeun pakait 63% [64]. ].99,9%) dina ngahasilkeun mimitian ti 58% nepi ka 76%, nu disintésis ku formasi beungkeut amida jeung rupa-rupa alkylamines ranté panjang atawa beungkeut éster jeung alkohol lemak ku Cbz-Arg-OMe, dimana papain acted salaku katalis.
5.2.2 Sintésis asam amino / péptida surfactants basis gémini
surfaktan Gemini dumasar-asam amino diwangun ku dua molekul AAS ranté lempeng numbu sirah-to-sirah ka silih ku grup spacer.Aya 2 kemungkinan skéma pikeun sintésis kémoénzimatik surfaktan dumasar-asam amino tipe gémini (Gambar 6 jeung 7).Dina Gambar 6, 2 turunan asam amino diréaksikeun jeung sanyawa salaku gugus spacer lajeng 2 gugus hidrofobik diwanohkeun.Dina Gambar 7, 2 struktur ranté lempeng langsung dikaitkeun babarengan ku grup spacer bifunctional.
Pangembangan pangheubeulna sintésis énzim-katalisis asam lipoamino Gemini ieu naratas ku Valivety et al.Yoshimura et al.nalungtik sintésis, adsorpsi jeung aggregation surfaktan gemini dumasar-asam amino dumasar kana cystine jeung n-alkil bromida.Surfaktan anu disintésis dibandingkeun sareng surfaktan monomérik anu aya.Faustino et al.ngajéntrékeun sintésis AAS monomérik berbasis uréa anionik dumasar kana L-cystine, D-cystine, DL-cystine, L-cysteine, L-methionine jeung L-sulfoalanine jeung pasangan gemini maranéhanana ku cara konduktivitas, tegangan permukaan kasaimbangan sarta ajeg. - kaayaan fluoresensi characterization sahijina.Ditémbongkeun yén nilai cmc gémini leuwih handap ku ngabandingkeun monomér jeung gémini.
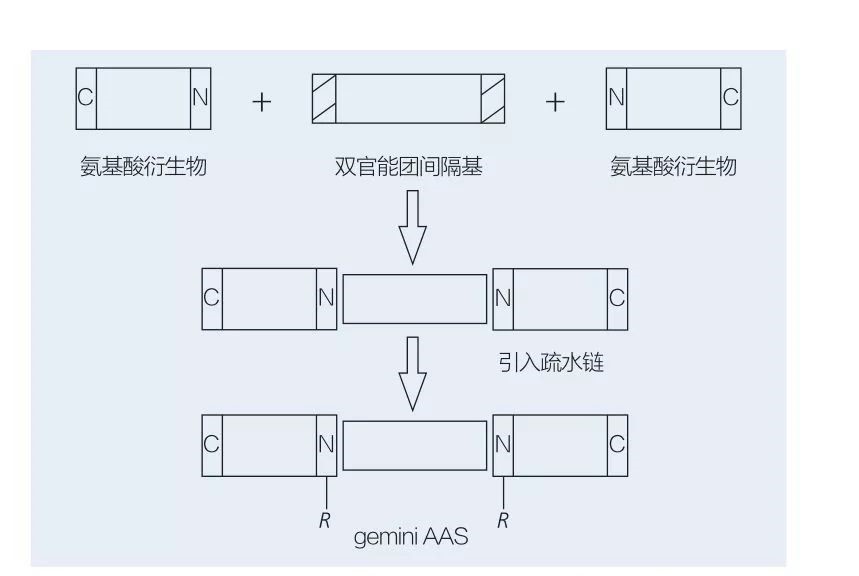
Gbr.6 Sintésis Gemini AAS maké turunan AA jeung spacer, dituturkeun ku sisipan gugus hidrofobik.
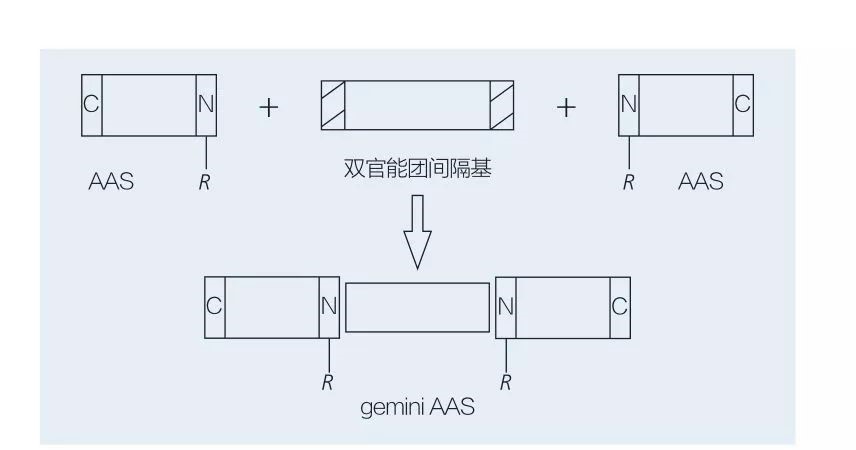
Gbr.7 Sintésis Gemini AASs maké spacer bifunctional na AAS
5.2.3 Sintésis asam amino gliserolipid/péptida surfaktan
Asam amino gliserolipid/péptida surfaktan téh kelas anyar asam amino lipid anu analog struktural gliserol mono- (atawa di-) éster jeung fosfolipid, alatan strukturna hiji atawa dua ranté lemak jeung hiji asam amino numbu ka tulang tonggong gliserol. ku beungkeut éster.Sintésis surfaktan ieu dimimitian ku persiapan gliserol éster asam amino dina suhu nu luhur jeung ku ayana katalis asam (misalna BF 3).Sintésis énzim-katalisis (ngagunakeun hidrolase, protease sareng lipase salaku katalis) ogé mangrupikeun pilihan anu saé (gambar 8).
Sintésis énzim-katalisis tina dilaurylated arginin gliserida conjugates maké papain geus dilaporkeun.Sintésis éster diasilgliserol konjugasi tina acetylarginine sareng evaluasi sipat fisikokimiana ogé parantos dilaporkeun.
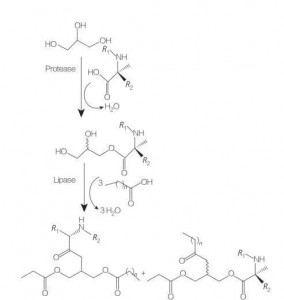
Gbr.8 Sintésis konjugat asam amino mono jeung diasilgliserol
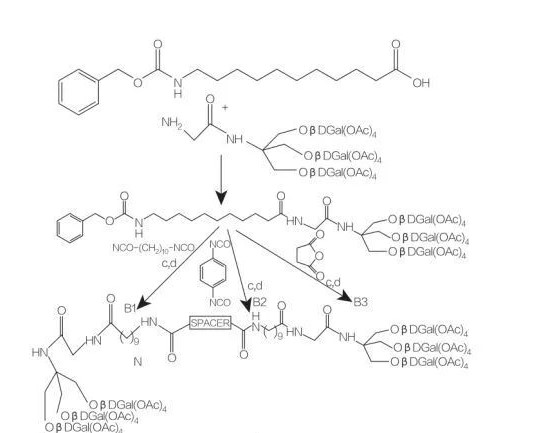
spacer: NH-(CH2)10-NH: sanyawa B1
spacer: NH-C6H4-NH: sanyawa B2
spacer: CH2-CH2: sanyawaB3
Gbr.9 Sintésis amfifil simetris diturunkeun tina Tris(hidroksimétil)aminometana
5.2.4 Sintésis asam amino / péptida surfaktan basis bola
Amfifil tipe bola dumasar asam amino ngandung 2 asam amino nu numbu ka ranté hidrofobik sarua.Franceschi et al.ngajéntrékeun sintésis amphiphiles tipe bola jeung 2 asam amino (D- atawa L-alanin atawa L-histidin) jeung 1 ranté alkil béda panjang sarta nalungtik aktivitas permukaan maranéhanana.Aranjeunna ngabahas sintésis jeung agrégasi amphiphiles tipe-bola novél jeung fraksi asam amino (ngagunakeun boh asam β-amino nu ilahar atawa alkohol) jeung grup spacer C12 -C20.Asam β-amino anu jarang dianggo tiasa janten asam amino gula, asam amino turunan azidothymin (AZT), asam amino norbornene, sareng alkohol amino anu diturunkeun tina AZT (Gambar 9).sintésis amphiphiles tipe bola simetris diturunkeun tina tris(hidroksimétil)aminometana (Tris) (Gambar 9).
06 Sipat fisikokimia
Perlu dipikanyaho yén surfaktan dumasar asam amino (AAS) rupa-rupa sareng serbaguna di alam sareng gaduh aplikasi anu saé dina seueur aplikasi sapertos solubilisasi anu saé, sipat émulsifikasi anu saé, efisiensi tinggi, kinerja kagiatan permukaan anu luhur sareng résistansi anu hadé pikeun cai teuas (ion kalsium). toleransi).
Dumasar kana sipat surfaktan asam amino (contona tegangan permukaan, cmc, paripolah fase sareng suhu Krafft), kacindekan di handap ieu kahontal saatos panilitian éksténsif - kagiatan permukaan AAS langkung unggul dibandingkeun sareng surfaktan konvensional.
6.1 Konsentrasi Misél Kritis (cmc)
Konsentrasi misel kritis mangrupikeun salah sahiji parameter penting surfaktan sareng ngatur seueur sipat aktif permukaan sapertos solubilisasi, lisis sél sareng interaksina sareng biofilm, jsb. dina nilai cmc leyuran surfactant, sahingga ngaronjatkeun aktivitas permukaan na.Surfaktan dumasar kana asam amino biasana mibanda nilai cmc nu leuwih handap dibandingkeun surfaktan konvensional.
Ngaliwatan kombinasi béda grup sirah jeung buntut hidrofobik (mono-cationic amida, bi-cationic amida, bi-cationic amida basis éster), Infante et al.disintésis tilu AAS basis arginin sarta diajar cmc maranéhanana jeung γcmc (tegangan permukaan dina cmc), némbongkeun yén nilai cmc jeung γcmc turun kalayan ngaronjatna panjang buntut hidrofobik.Dina ulikan sejen, Singare jeung Mhatre manggihan yén cmc surfaktan N-α-asilarginin turun kalayan ngaronjatna jumlah atom karbon buntut hidrofobik (Tabel 1).
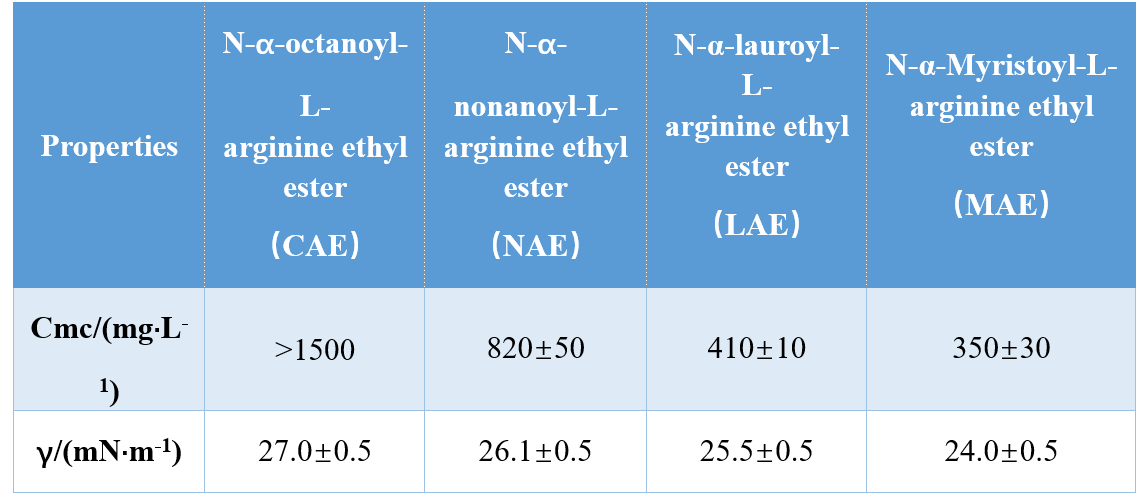
Yoshimura et al.nalungtik cmc tina surfaktan gémini dumasar asam amino sistein-turunan sarta némbongkeun yén cmc nu turun nalika panjang ranté karbon dina ranté hidrofobik ngaronjat tina 10 ka 12. Salajengna ngaronjatna panjang ranté karbon ka 14 nyababkeun kanaékan cmc, nu dikonfirmasi yén surfaktan gemini ranté panjang boga kacenderungan handap pikeun agrégat.
Faustino et al.dilaporkeun formasi micelles dicampur dina leyuran cai surfaktan gemini anionik dumasar kana cystine.Surfaktan gémini ogé dibandingkeun sareng surfaktan monomérik konvensional (C 8 Cys).Nilai cmc tina campuran lipid-surfaktan dilaporkeun leuwih handap tina surfaktan murni.surfaktan gemini jeung 1,2-diheptanoyl-sn-glyceryl-3-phosphocholine, larut cai, fosfolipid ngabentuk misel, miboga cmc dina tingkat milimolar.
Shrestha jeung Aramaki nalungtik formasi micelles kawas cacing viscoelastic dina leyuran cai surfaktan anionik-nonionik dumasar-asam amino dina henteuna uyah admixture.Dina ulikan ieu, N-dodecyl glutamat kapanggih boga suhu Krafft luhur;kumaha oge, nalika nétralisasi ku asam amino L-lisin dasar, éta ngahasilkeun misel jeung leyuran mimiti berperilaku kawas cairan Newtonian dina 25 °C.
6.2 kaleyuran cai alus
Kalarutan cai anu hadé tina AAS disababkeun ku ayana beungkeut CO-NH tambahan.Hal ieu ngajadikeun AAS leuwih biodegradable tur ramah lingkungan ti surfactants konvensional pakait.Kalarutan cai asam N-asil-L-glutamat langkung saé kusabab 2 gugus karboksil na.Kalarutan cai tina Cn(CA) 2 ogé alus sabab aya 2 gugus arginin ionik dina 1 molekul, nu ngakibatkeun adsorpsi jeung difusi leuwih éféktif dina panganteur sél jeung malah inhibisi baktéri éféktif dina konsentrasi handap.
6.3 Suhu Krafft jeung titik Krafft
Suhu Krafft bisa dipikaharti salaku paripolah kaleyuran spésifik surfaktan anu kaleyuranna naék saluhureun suhu nu tangtu.Surfaktan ionik boga kacenderungan pikeun ngahasilkeun hidrat padet, nu bisa présipitasi kaluar tina cai.Dina suhu nu tangtu (nu disebut suhu Krafft), paningkatan dramatis jeung discontinuous dina kaleyuran surfaktan biasana ditempo.Titik Krafft surfaktan ionik nyaéta suhu Krafft na dina cmc.
Karakteristik kalarutan ieu biasana ditingali pikeun surfaktan ionik sareng tiasa dijelaskeun kieu: kaleyuran monomér bébas surfaktan diwatesan di handap suhu Krafft dugi ka titik Krafft ngahontal, dimana kalarutanna laun-laun naék alatan formasi misel.Pikeun mastikeun kaleyuran lengkep, perlu nyiapkeun formulasi surfactant dina suhu luhur titik Krafft.
Suhu Krafft AAS parantos ditalungtik sareng dibandingkeun sareng surfaktan sintétik konvensional. ×10-6 mol-L -1 dituturkeun ku formasi micelle normal (Ohta et al. disintésis genep tipena béda N-hexadecanoyl AAS jeung ngabahas hubungan antara suhu Krafft maranéhanana jeung résidu asam amino.
Dina percobaan, éta kapanggih yén suhu Krafft of N-hexadecanoyl AAS ngaronjat kalawan ukuran nurunna résidu asam amino (phenylalanine jadi pangecualian), sedengkeun panas kaleyuran (panas uptake) ngaronjat kalayan ukuran nurunna résidu asam amino (jeung iwal glisin sareng fenilalanin).Disimpulkeun yén dina sistem alanin sareng fenilalanin, interaksi DL langkung kuat tibatan interaksi LL dina bentuk padet uyah N-hexadecanoyl AAS.
Brito et al.nangtukeun suhu Krafft tina tilu runtuyan surfaktan dumasar-asam amino novél ngagunakeun diferensial scanning microcalorimetry sarta manggihan yén ngarobah ion trifluoroacetate kana ion iodide nyababkeun kanaékan signifikan dina suhu Krafft (kira 6 °C), ti 47 °C nepi ka 53 °. C.Ayana beungkeut cis-ganda sareng henteu jenuh anu aya dina turunan Ser-rantai panjang nyababkeun panurunan anu signifikan dina suhu Krafft.n-Dodecyl glutamat dilaporkeun mibanda suhu Krafft nu leuwih luhur.Tapi, nétralisasi jeung asam amino L-lisin dasar ngahasilkeun misél dina leyuran nu behave kawas cairan Newtonian dina 25 °C.
6.4 Tegangan permukaan
Tegangan permukaan surfaktan patali jeung panjang ranté bagian hidrofobik.Zhang et al.nangtukeun tegangan permukaan natrium cocoyl glycinate ku metoda Wilhelmy plate (25±0.2) ° C jeung nangtukeun nilai tegangan permukaan dina cmc salaku 33 mN-m -1, cmc salaku 0.21 mmol-L -1.Yoshimura et al.nangtukeun tegangan permukaan 2C n Cys tipe asam amino tegangan permukaan dumasar kana 2C n Cys dumasar permukaan agén aktip.Ieu kapanggih yén tegangan permukaan dina cmc turun kalayan ngaronjatna panjang ranté (dugi ka n = 8), bari trend ieu dibalikkeun pikeun surfactants kalawan n = 12 atawa panjang ranté panjang.
Pangaruh CaC1 2 dina tegangan permukaan surfaktan dumasar-asam amino dikarboksilasi ogé parantos ditaliti.Dina studi ieu, CaC1 2 ditambahkeun kana larutan cai tina tilu surfaktan tipe asam amino dikarboksilasi (C12 MalNa 2, C12 AspNa 2, jeung C12 GluNa 2).Nilai dataran sanggeus cmc dibandingkeun jeung kapanggih yén tegangan permukaan turun dina konsentrasi CaC1 2 pisan low.Ieu alatan pangaruh ion kalsium dina susunan surfactant dina panganteur gas-cai.tegangan permukaan uyah N-dodecylaminomalonate na N-dodecylaspartate, di sisi séjén, ogé ampir konstan nepi ka 10 mmol-L -1 konsentrasi CaC1 2.Di luhur 10 mmol-L -1, tegangan permukaan ningkat sacara signifikan, kusabab kabentukna présipitasi uyah kalsium surfaktan.Pikeun uyah disodium N-dodecyl glutamat, tambahan sedeng CaC1 2 nyababkeun panurunan anu signifikan dina tegangan permukaan, sedengkeun paningkatan konsentrasi CaC1 2 henteu deui nyababkeun parobahan anu signifikan.
Pikeun nangtukeun kinétika adsorpsi tina Gemini-tipe AAS dina panganteur gas-cai, tegangan permukaan dinamis ditangtukeun ngagunakeun métode tekanan gelembung maksimum.Hasilna nunjukkeun yén pikeun waktos uji pangpanjangna, tegangan permukaan dinamis 2C 12 Cys henteu robih.Turunna tegangan permukaan dinamis ngan ukur gumantung kana konsentrasi, panjang buntut hidrofobik, sareng jumlah buntut hidrofobik.Ngaronjatna konsentrasi surfaktan, nurunna panjang ranté ogé jumlah ranté nyababkeun burukna langkung gancang.Hasilna diala pikeun konsentrasi luhur C n Cys (n = 8 nepi ka 12) kapanggih deukeut pisan jeung γ cmc diukur ku métode Wilhelmy.
Dina ulikan sejen, tegangan permukaan dinamis natrium dilauryl cystine (SDLC) jeung natrium didecamino cystine ditangtukeun ku metoda Wilhelmy plat, jeung sajaba ti éta, tegangan permukaan kasatimbangan solusi cai maranéhanana ditangtukeun ku metoda volume serelek.Réaksi beungkeut disulfida ditalungtik satuluyna ku métode séjénna ogé.Penambahan mercaptoethanol kana 0,1 mmol-L -1SDLC solusi nyababkeun kanaékan gancang dina tegangan permukaan ti 34 mN-m -1 mun 53 mN-m -1.Kusabab NaClO tiasa ngoksidasi beungkeut disulfida SDLC kana gugus asam sulfonat, henteu aya agrégat nalika NaClO (5 mmol-L -1) ditambahkeun kana larutan SDLC 0,1 mmol-L -1.Transmisi mikroskop éléktron jeung hasil scattering lampu dinamis némbongkeun yén euweuh aggregates kabentuk dina leyuran.Tegangan permukaan SDLC kapanggih ningkat tina 34 mN-m -1 ka 60 mN-m -1 salami 20 mnt.
6.5 Interaksi permukaan binér
Dina élmu kahirupan, sajumlah grup geus nalungtik sipat geter campuran AAS kationik (surfaktan dumasar-diasilgliserol arginin) jeung fosfolipid dina panganteur gas-cai, tungtungna menyimpulkan yén sipat non-idéal ieu ngabalukarkeun Prévalénsi interaksi éléktrostatik.
6.6 sipat Aggregation
Paburencay cahaya dinamis ilaharna dipaké pikeun nangtukeun sipat agrégasi monomér dumasar-asam amino jeung surfaktan gémini dina konsentrasi luhur cmc, ngahasilkeun DH diaméter hidrodinamik semu (= 2R H ).Agrégat nu dibentuk ku C n Cys jeung 2Cn Cys rélatif badag sarta miboga sebaran skala lega dibandingkeun surfactants lianna.Kabéh surfaktan iwal 2C 12 Cys ilaharna ngabentuk agrégat ngeunaan 10 nm.ukuran misel surfaktan gemini nyata leuwih badag batan ukuran monomérikna.Paningkatan panjang ranté hidrokarbon ogé ngabalukarkeun kanaékan ukuran misel.ohta et al.ngajéntrékeun sipat agrégasi tilu stereoisomer béda N-dodecyl-phenyl-alanyl-phenyl-alanine tetramethylammonium dina leyuran cai sarta némbongkeun yén diastereoisomers boga konsentrasi aggregation kritis sarua dina leyuran cai.Iwahashi et al.ditalungtik ku dichroism sirkular, NMR jeung tekanan uap osmometry nu Kabentukna agrégat kiral asam N-dodecanoyl-L-glutamat, N-dodecanoyl-L-valina jeung métil éster maranéhanana dina pangleyur béda (kayaning tetrahydrofuran, acetonitrile, 1,4). -dioxane jeung 1,2-dikloroetana) mibanda sipat rotasi ieu ditalungtik ku dichroism sirkular, NMR jeung tekanan uap osmometry.
6.7 Adsorption panganteur
Adsorpsi antarbeungeut surfaktan dumasar-asam amino sareng babandinganana sareng pasangan konvensionalna ogé mangrupikeun salah sahiji arah panalungtikan.Salaku conto, sipat adsorpsi antarbeungeut éster dodecyl asam amino aromatik anu dicandak tina LET sareng LEP ditalungtik.Hasilna nunjukkeun yén LET sareng LEP nunjukkeun daérah antarmuka anu langkung handap dina antarmuka gas-cair sareng dina antarmuka cai / heksana, masing-masing.
Bordes et al.nalungtik paripolah solusi jeung adsorpsi dina panganteur gas-cai tina tilu surfaktan asam amino dikarboksilasi, uyah disodium tina dodecyl glutamat, dodecyl aspartate, jeung aminomalonate (jeung 3, 2, jeung 1 atom karbon antara dua gugus karboksil, masing-masing).Numutkeun laporan ieu, cmc surfaktan dikarboksilasi éta 4-5 kali leuwih luhur batan uyah dodesil glisin monokarboksilasi.Ieu dikaitkeun kana kabentukna beungkeut hidrogén antara surfaktan dikarboksilasi jeung molekul tatangga ngaliwatan gugus amida di jerona.
6.8 Fase kabiasaan
Fase kubik discontinuous isotropik dititénan pikeun surfaktan dina konsentrasi kacida luhurna.Molekul surfaktan kalayan gugus sirah anu kacida gedéna condong ngabentuk agrégat tina kelengkungan positip anu leuwih leutik.marques et al.nalungtik paripolah fase sistem 12Lys12 / 12Ser na 8Lys8 / 16Ser (tingali Gambar 10), sarta hasil némbongkeun yén sistem 12Lys12 / 12Ser ngabogaan zone pamisahan fase antara wewengkon solusi micellar na vesicular, sedengkeun sistem 8Lys8 / 16Ser The Sistim 8Lys8/16Ser nembongkeun transisi kontinyu (wewengkon fase micellar elongated antara wewengkon fase micellar leutik jeung wewengkon fase vesicle).Perlu dicatet yén pikeun daérah vesikel sistem 12Lys12/12Ser, vesikel sok aya babarengan jeung micelles, sedengkeun wewengkon vesikel sistem 8Lys8/16Ser ngan boga vesikel.
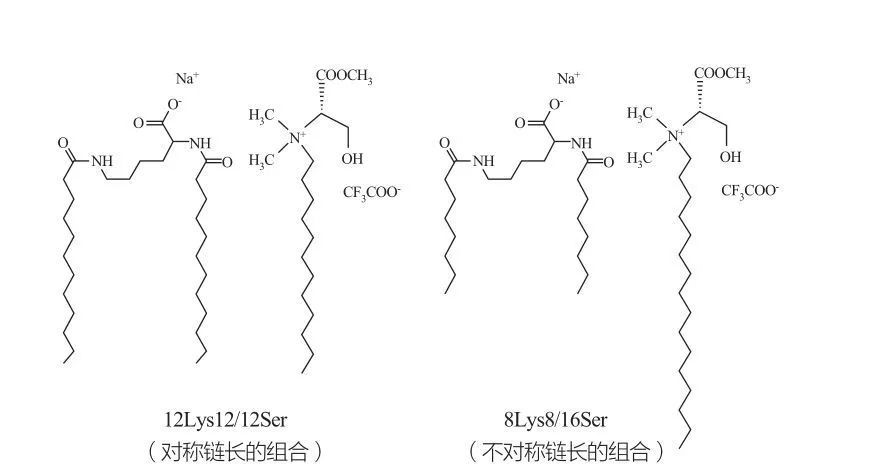
Campuran kataoninik tina surfaktan dumasar kana lisin sareng serin: simetris 12Lys12/12Ser pasangan (kénca) jeung asimétri 8Lys8/16Ser pasangan (katuhu)
6.9 Kamampuhan émulsi
Kouchi et al.nalungtik kamampuh emulsifying, tegangan panganteur, dispersibility, sarta viskositas N-[3-dodecyl-2-hydroxypropyl]-L-arginine, L-glutamat, sarta AAS lianna.Dibandingkeun sareng surfaktan sintétik (nonionik sareng amphotérik konvensionalna), hasil nunjukkeun yén AAS gaduh kamampuan émulsi anu langkung kuat tibatan surfaktan konvensional.
Baczko et al.nyintésis surfaktan asam amino anionik novél sareng nalungtik kasesuaianna salaku pangleyur spéktroskopi NMR berorientasi kiral.Runtuyan turunan amfifilik L-Phe atawa L-Ala dumasar sulfonat kalawan buntut hidrofobik anu béda (pentyl~tetradecyl) disintésis ku ngaréaksikeun asam amino jeung anhidrida o-sulfobenzoat.Wu et al.disintésis uyah natrium N-lemak asil AAS jeungnalungtik kamampuh émulsifikasi maranéhanana dina minyak-dina-cai emulsions, sarta hasil némbongkeun yén surfaktan ieu kinerja hadé kalawan étil asetat salaku fase minyak ti kalayan n-héksana salaku fase minyak.
6.10 Kamajuan dina sintésis jeung produksi
Résistansi cai teuas bisa dipikaharti salaku kamampuh surfaktan pikeun nolak ayana ion kayaning kalsium jeung magnésium dina cai teuas, nyaéta kamampuhan pikeun nyingkahan présipitasi kana sabun kalsium.Surfaktan kalawan résistansi cai teuas anu pohara kapaké pikeun formulasi detergent jeung produk perawatan pribadi.Résistansi cai teuas bisa dievaluasi ku ngitung parobahan dina kaleyuran jeung aktivitas permukaan surfaktan ku ayana ion kalsium.
Cara séjén pikeun ngira-ngira résistansi cai teuas nyaéta ngitung persentase atawa gram surfaktan anu diperlukeun pikeun sabun kalsium anu kabentuk tina 100 g natrium oleate pikeun dispersed dina cai.Di wewengkon kalawan cai teuas luhur, konsentrasi luhur ion kalsium jeung magnesium sarta kandungan mineral bisa nyieun sababaraha aplikasi praktis hésé.Mindeng ion natrium dipaké salaku counter ion surfaktan anionik sintétik.Kusabab ion kalsium divalén kabeungkeut kana duanana molekul surfaktan, éta ngabalukarkeun surfaktan pikeun éndapan leuwih gampang tina solusi nyieun detergénsi kurang kamungkinan.
Ulikan ngeunaan résistansi cai teuas AAS némbongkeun yén résistansi asam jeung cai teuas dipangaruhan pisan ku gugus karboksil tambahan, sarta résistansi asam jeung cai teuas ngaronjat deui kalawan ngaronjatna panjang gugus spacer antara dua gugus karboksil. .Urutan résistansi asam jeung cai teuas nyaéta C 12 glisinat < C 12 aspartat < C 12 glutamat.Ngabandingkeun beungkeut amida dikarboksilasi sareng surfaktan amino dikarboksilasi, masing-masing, kapanggih yén kisaran pH anu terakhir langkung lega sareng kagiatan permukaanna ningkat kalayan ditambahan jumlah asam anu pas.Asam amino N-alkil dikarboksilasi nunjukkeun pangaruh chelating ku ayana ion kalsium, sareng C 12 aspartate ngabentuk gél bodas.c 12 glutamat nunjukkeun aktivitas permukaan anu luhur dina konsentrasi Ca 2+ anu luhur sareng diperkirakeun dianggo dina desalinasi cai laut.
6.11 Dispersibility
Dispersibility nujul kana kamampuh hiji surfactant pikeun nyegah coalescence sarta sedimentasi surfactant dina leyuran.Dispersibility mangrupikeun sipat penting tina surfaktan anu ngajantenkeun aranjeunna cocog pikeun dianggo dina deterjen, kosmétik sareng farmasi.Agén panyebar kudu ngandung beungkeut éster, éter, amida atawa amino antara gugus hidrofobik jeung gugus hidrofilik terminal (atawa diantara gugus hidrofobik ranté lempeng).
Sacara umum, surfaktan anionik sapertos alkanolamido sulfat sareng surfaktan amfoter sapertos amidosulfobetaine sabagian efektif salaku agén panyebarkeun sabun kalsium.
Loba usaha panalungtikan geus ditangtukeun dispersibility of AAS, dimana N-lauroyl lisin kapanggih kirang cocog jeung cai sarta hésé dipaké pikeun formulasi kosmetik.Dina séri ieu, asam amino dasar anu disubstitusi N-asil gaduh dispersibilitas anu saé sareng dianggo dina industri kosmetik pikeun ningkatkeun formulasi.
07 Karacunan
Surfaktan konvensional, utamana surfaktan kationik, kacida toksik pikeun organisme akuatik.Toksisitas akut maranéhanana disababkeun ku fenomena interaksi adsorption-ion surfactants dina panganteur sél-cai.Nurunkeun cmc surfaktan biasana ngakibatkeun adsorpsi antarmuka surfaktan anu langkung kuat, anu biasana nyababkeun karacunan akut anu luhur.Paningkatan dina panjang ranté hidrofobik surfaktan ogé ngabalukarkeun kanaékan karacunan akut surfaktan.Kaseueuran AAS rendah atanapi henteu beracun pikeun manusa sareng lingkungan (khususna pikeun organisme laut) sareng cocog pikeun dianggo salaku bahan pangan, farmasi sareng kosmétik.Seueur panaliti nunjukkeun yén surfaktan asam amino lembut sareng henteu ngaganggu kulit.Surfaktan dumasar-arginin dipikanyaho kirang beracun tibatan anu biasa.
Brito et al.nalungtik sipat fisikokimia jeung toksikologis amphiphiles dumasar-asam amino sarta maranéhanana [turunan tina tirosin (Tyr), hydroxyproline (Hyp), serine (Ser) jeung lisin (Lys)] formasi spontan vesikel kationik maranéhanana sarta méré data ngeunaan karacunan akut maranéhanana. Daphnia magna (IC 50).Aranjeunna disintésis vesikel kationik tina dodecyltrimethylammonium bromide (DTAB)/Lys-turunan jeung/atawa campuran Ser-/Lys-turunan sarta nguji ékotoksisitas sarta poténsi hemolitik maranéhanana, némbongkeun yén sakabéh AAS jeung campuran vesicle-ngandung maranéhanana éta kirang toksik batan surfaktan DTAB konvensional. .
Rosa et al.nalungtik beungkeutan (asosiasi) DNA ka vésikel kationik basis asam amino stabil.Teu kawas surfaktan kationik konvensional, nu mindeng kaciri toksik, interaksi surfaktan asam amino kationik sigana non-toksik.AAS kationik dumasar kana arginin, anu sacara spontan ngabentuk vesikel stabil dina kombinasi sareng surfaktan anionik.Inhibitor korosi dumasar-asam amino ogé dilaporkeun henteu beracun.surfaktan ieu gampang disintésis kalawan purity tinggi (nepi ka 99%), béaya rendah, gampang biodegradable, sarta sagemblengna leyur dina media cai.Sababaraha panilitian nunjukkeun yén surfaktan asam amino anu ngandung walirang langkung unggul dina ngahambat korosi.
Dina ulikan panganyarna, Perinelli et al.dilaporkeun profil toksikologis nyugemakeun rhamnolipids dibandingkeun surfactants konvensional.Rhamnolipids dipikanyaho meta salaku enhancer perméabilitas.Éta ogé ngalaporkeun pangaruh rhamnolipids dina perméabilitas épitél ubar makromolekul.
08 Kagiatan antimikrobial
Aktivitas antimikrobial surfaktan tiasa dievaluasi ku konsentrasi panghambat minimum.Aktivitas antimikrobial surfaktan dumasar-arginin parantos ditaliti sacara rinci.Baktéri Gram-négatip kapanggih leuwih tahan ka surfaktan dumasar-arginin batan baktéri Gram-positip.Aktivitas antimikroba surfaktan biasana ngaronjat ku ayana beungkeut hidroksil, siklopropana atawa teu jenuh dina ranté asil.Castillo et al.némbongkeun yén panjang ranté asil jeung muatan positif nangtukeun nilai HLB (hidrofilik-lipofilik kasaimbangan) molekul, sarta ieu boga pangaruh dina kamampuhan pikeun ngaganggu mémbran.Nα-acylarginine métil éster nyaéta kelas penting séjén surfaktan kationik kalawan spéktrum lega aktivitas antimikrobial sarta Éta gampang biodegradable sarta boga karacunan low atawa euweuh.Studi ngeunaan interaksi surfaktan basis Nα-asilarginin métil éster kalawan 1,2-dipalmitoyl-sn-propyltrioxyl-3-phosphorylcholine jeung 1,2-ditetradecanoyl-sn-propyltrioxyl-3-phosphorylcholine, model mémbran, jeung organisme hirup di Ayana atanapi henteuna halangan éksternal nunjukkeun yén kelas surfaktan ieu ngagaduhan antimikrobial anu saé. Hasilna nunjukkeun yén surfaktan gaduh kagiatan antibakteri anu saé.
09 Sipat réologis
Sipat réologis surfaktan maénkeun peran anu penting pisan dina nangtukeun sareng ngaramal aplikasina dina industri anu béda, kalebet tuangeun, farmasi, ékstraksi minyak, perawatan pribadi sareng produk perawatan bumi.Seueur panilitian anu dilakukeun pikeun ngabahas hubungan antara viskoelastisitas surfaktan asam amino sareng cmc.
10 Aplikasi dina industri kosmetik
AAS dianggo dina ngarumuskeun seueur produk perawatan pribadi.kalium N-cocoyl glycinate kapanggih janten hipu dina kulit sarta dipaké dina cleansing raray pikeun miceun sludge jeung makeup.Asam n-Acyl-L-glutamat boga dua gugus karboksil, nu ngajadikeun eta leuwih leyur dina cai.Diantara AAS ieu, AAS dumasar kana asam lemak C 12 seueur dianggo dina ngabersihkeun raray pikeun ngaleungitkeun sludge sareng makeup.AAS sareng ranté C 18 dianggo salaku pangémulsi dina produk perawatan kulit, sareng uyah N-Lauryl alanin dipikanyaho nyiptakeun busa krim anu henteu ngairitasi kulit sahingga tiasa dianggo dina ngarumuskeun produk perawatan orok.N-Lauryl basis AAS dipaké dina odol boga detergency alus sarupa sabun jeung kuat énzim-inhibiting efficacy.
Sapanjang sababaraha dekade katukang, pilihan surfaktan pikeun kosmétik, produk perawatan pribadi sareng farmasi parantos museurkeun kana karacunan anu rendah, kalemahan, kelembutan pikeun kabaran sareng kaamanan.Konsumén produk ieu sadar pisan kana poténsi iritasi, karacunan sareng faktor lingkungan.
Kiwari, AAS dianggo pikeun ngarumuskeun seueur shampoos, pewarna rambut sareng sabun mandi kusabab seueur kaunggulanna dibandingkeun sareng kosmétik tradisional sareng produk perawatan pribadi.Surfaktan dumasar-protéin gaduh sipat anu dipikahoyong anu dipikabutuh pikeun produk perawatan pribadi.Sababaraha AAS gaduh kamampuan ngabentuk pilem, sedengkeun anu sanésna gaduh kamampuan busa anu saé.
Asam amino mangrupikeun faktor pelembab alami anu penting dina stratum korneum.Nalika sél épidermis maot, aranjeunna janten bagian tina stratum korneum sareng protéin intrasélular laun-laun didegradasi janten asam amino.Asam amino ieu teras diangkut langkung jauh kana stratum corneum, dimana aranjeunna nyerep lemak atanapi zat sapertos lemak kana stratum corneum épidermis, ku kituna ningkatkeun élastisitas permukaan kulit.Kira-kira 50% faktor pelembab alami dina kulit diwangun ku asam amino sareng pirolidon.
Kolagén, bahan kosmetik umum, ogé ngandung asam amino anu ngajaga kulit lemes.Masalah kulit sapertos kasar sareng kusam disababkeun sabagian ageung kusabab kakurangan asam amino.Hiji studi némbongkeun yén campur asam amino jeung salep lega kaduruk kulit, sarta wewengkon nu dimaksud balik deui ka kaayaan normal maranéhanana tanpa jadi scars keloid.
Asam amino ogé geus kapanggih pisan mangpaat dina miara cuticles ruksak.Rambut anu garing sareng teu aya wujudna tiasa nunjukkeun panurunan dina konsentrasi asam amino dina stratum corneum anu ruksak parah.Asam amino gaduh kamampuan pikeun nembus kutikula kana aci rambut sareng nyerep Uap tina kulit.Kamampuhan ieu surfaktan dumasar asam amino ngajadikeun eta pohara kapaké dina shampoos, dyes bulu, softeners bulu, kondisioner bulu, sarta ayana asam amino ngajadikeun bulu kuat.
11 Aplikasi dina kosmétik sapopoé
Ayeuna, aya paménta tumuwuh pikeun formulasi detergent basis asam amino di sakuliah dunya.AAS dipikanyaho gaduh kamampuan beberesih anu langkung saé, kamampuan berbusa sareng sipat ngalembutkeun lawon, anu ngajantenkeun aranjeunna cocog pikeun detergent rumah tangga, sampo, cuci awak sareng aplikasi anu sanés.Hiji AAS amfoteric turunan asam aspartat dilaporkeun janten detergent kacida mujarab jeung sipat chelating.Pamakéan bahan deterjen anu diwangun ku asam N-alkil-β-aminoethoxy kapanggih pikeun ngurangan iritasi kulit.Formulasi deterjen cair anu diwangun ku N-cocoyl-β-aminopropionate parantos dilaporkeun janten detergent anu mujarab pikeun noda minyak dina permukaan logam.Hiji surfaktan asam aminokarboksilat, C 14 CHOHCH 2 NHCH 2 COONa, ogé geus kabuktian boga detergénsi hadé tur dipaké pikeun meresihan tékstil, karpét, bulu, kaca, jsb The 2-hidroksi-3-aminopropionic acid-N,N- Turunan asam acetoacetic dipikanyaho gaduh kamampuan komplek anu saé sahingga masihan stabilitas kana agén pemutihan.
Nyiapkeun formulasi detergent dumasar kana N-(N'-long-chain acyl-β-alanyl)-β-alanine geus dilaporkeun ku Keigo jeung Tatsuya dina patén maranéhna pikeun kamampuhan cuci hadé tur stabilitas, gampang megatkeun busa jeung softening lawon alus. .Kao ngembangkeun formulasi detergent dumasar kana N-Acyl-1 -N-hydroxy-β-alanine sarta ngalaporkeun iritasi kulit low, résistansi cai luhur jeung kakuatan panyabutan noda tinggi.
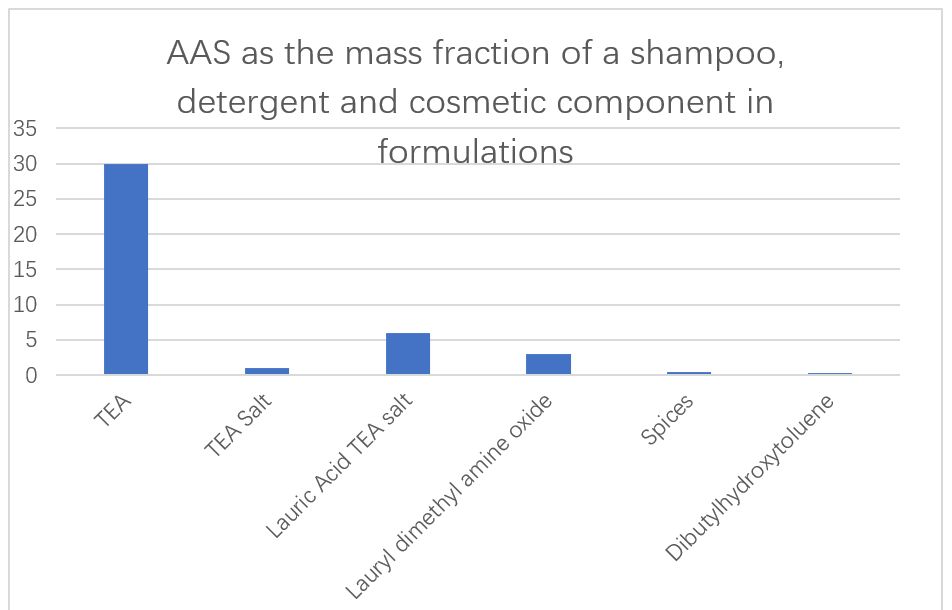
Pausahaan Jepang Ajinomoto ngagunakeun AAS low-toksik jeung gampang degradable dumasar kana asam L-glutamat, L-arginin jeung L-lisin salaku bahan utama dina shampoos, detergents jeung kosmétik (Gambar 13).Kamampuh aditif énzim dina formulasi detergent pikeun ngaleungitkeun fouling protéin ogé geus dilaporkeun.N-asil AAS diturunkeun tina asam glutamat, alanin, methylglycine, serine jeung asam aspartat geus dilaporkeun pikeun pamakéan maranéhanana salaku detergents cair alus teuing dina leyuran cai.Surfactants ieu teu ningkatkeun viskositas pisan, sanajan dina suhu pisan low, sarta bisa gampang ditransfer ti wadah panyimpen alat foaming pikeun ménta foams homogen.
waktos pos: Jun-09-2022

